Dans quelle mesure l’alimentation peut-elle moduler les mécanismes endogènes de détoxification, et quelles sont les limites biologiques de cette modulation ?
Contenu de l'article
ToggleProblématique de la détox
La « détox » ou détoxification alimentaire s’est imposée comme l’un des concepts nutritionnels les plus médiatisés de la dernière décennie. Cures de jus pressés à froid, jeûnes protocolisés, mono-diètes à base de légumes verts, compléments alimentaires aux noms évocateurs… Le marché mondial de la détox est estimé à plusieurs milliards d’euros, porté par une promesse simple : celle de « nettoyer » l’organisme des toxines accumulées par une alimentation moderne trop riche, trop transformée, trop polluée.
Pourtant, à la lumière de la biochimie, cette promesse se heurte immédiatement à une question fondamentale : de quelles « toxines » parle-t-on précisément ? Et si l’organisme dispose depuis des millions d’années de systèmes enzymatiques hautement performants pour neutraliser et éliminer les xénobiotiques, qu’apporte réellement une cure de trois jours au jus de céleri ?
C’est à cette question, à la fois scientifique et clinique, que nous allons tenter de répondre dans cet article. L’objectif n’est pas de disqualifier en bloc toute approche nutritionnelle visant à soutenir les voies d’élimination de l’organisme — certaines ont un réel fondement biochimique — mais de distinguer avec rigueur ce qui relève de la physiologie documentée de ce qui appartient au registre du marketing et de l’effet de mode, voire à celui d’un idéal de « purification » du corps. Soyons rationnels pour démêler Détox et Intox.
Ce que la biologie entend vraiment par « détoxification » ou « détox »
Les toxines : de quoi parle-t-on ?
Un être humain vit dans un environnement où il est exposé à de nombreuses substances étrangères : les xénobiotiques. Ils sont issus des médicaments, des polluants, de la fumée de cigarette, des additifs et des contaminants alimentaires issus des aliments et des boissons naturels ou transformés (alcool ou métabolites bactériens par exemple)
Ces xénobiotiques ont vocation à être détectés puis éliminés du corps par des mécanismes physiologiques compétents.
Par ailleurs, de nombreuses substances endogènes sont générées par les différents métabolismes du corps humain lui-même ; ce sont des molécules issues de nos propres synthèses : hormones stéroïdiennes, acides biliaires, acides gras, prostaglandines et autres dérivés des eicosanoïdes, …. Se pose ici la question de leur élimination, qui permet de réguler leur activité.
Toutes ces substances peuvent être soit hydrophiles (solubles dans l’eau) soit hydrophobes (non solubles dans l’eau). Les composés hydrophiles sont facilement véhiculés par le sang puis éliminés par l’urine, la bile, la sueur ou la respiration. La difficulté réside dans l’élimination des produits hydrophobes, non directement compatibles avec ces voies d’élimination.
Pour résoudre cette difficulté, l’organisme dispose de capacités enzymatiques très sophistiquées, qui permettent de transformer ces composés hydrophobes en produits (« métabolites ») hydrophiles qui seront facilement éliminés par les voies déjà citées.
Ce sont ces xénobiotiques et composés endogènes que l’on nomme dans le langage courant « toxines », et ces réactions de biotransformation constituent notre système de traitement appelé « détoxification » endogène.
Avant de parler de « détox alimentaire », la compréhension de ce système de biotransformation est indispensable à toute discussion rationnelle sur le sujet.
Les organes impliqués et leur rôle physiologique
Le foie est l’organe central de la biotransformation. Il reçoit en premier lieu, via la veine porte, l’ensemble des molécules absorbées par le tractus gastro-intestinal. Grâce à sa richesse en enzymes spécialisées — au premier rang desquelles les cytochromes P450 — il transforme chimiquement, via les phases I et II, les xénobiotiques hydrophobes (non solubles dans l’eau) en composés (métabolites) hydrosolubles (solubles dans l’eau), et donc pouvant ensuite être excrétés (éliminés) par le corps. Ce processus, appelé biotransformation, ne doit pas être confondu avec une simple « neutralisation » : certains composés sont activés avant d’être désactivés, ce qui implique des risques si certaines étapes sont déficientes.
Le rein assure la filtration glomérulaire et l’excrétion urinaire des métabolites hydrosolubles issus de la biotransformation hépatique, ainsi que des substances directement filtrables (urée, créatinine, acide urique, certains médicaments). Son bon fonctionnement est directement conditionné par le statut d’hydratation.
L’intestin ne constitue pas seulement une voie d’absorption : il représente une barrière de premier rang face aux antigènes alimentaires et aux xénobiotiques. Les entérocytes expriment eux-mêmes des enzymes de phase I et II, et les transporteurs membranaires de la famille ABC (dont la P-glycoprotéine) limitent l’absorption de nombreuses molécules potentiellement nocives. L’excrétion biliaire, relayée par les selles, constitue également une voie majeure d’élimination des composés lipophiles conjugués.
La peau (via la sudation) et les poumons (via l’air expiré) contribuent de façon marginale mais non négligeable à l’élimination de certains composés volatils ou liposolubles.
| EN PRATIQUE — Ce qu’on doit retenir |
| L’organisme détoxifie en permanence, sans interruption, grâce à des systèmes enzymatiques hautement régulés. |
| Ces systèmes ne s’arrêtent pas lors d’une « mauvaise période alimentaire » et ne nécessitent pas de cure spécifique pour fonctionner. |
| La question pertinente n’est pas « faut-il se détoxifier ? » mais « mon alimentation fournit-elle les facteurs nécessaires au bon fonctionnement de ces systèmes ? » |
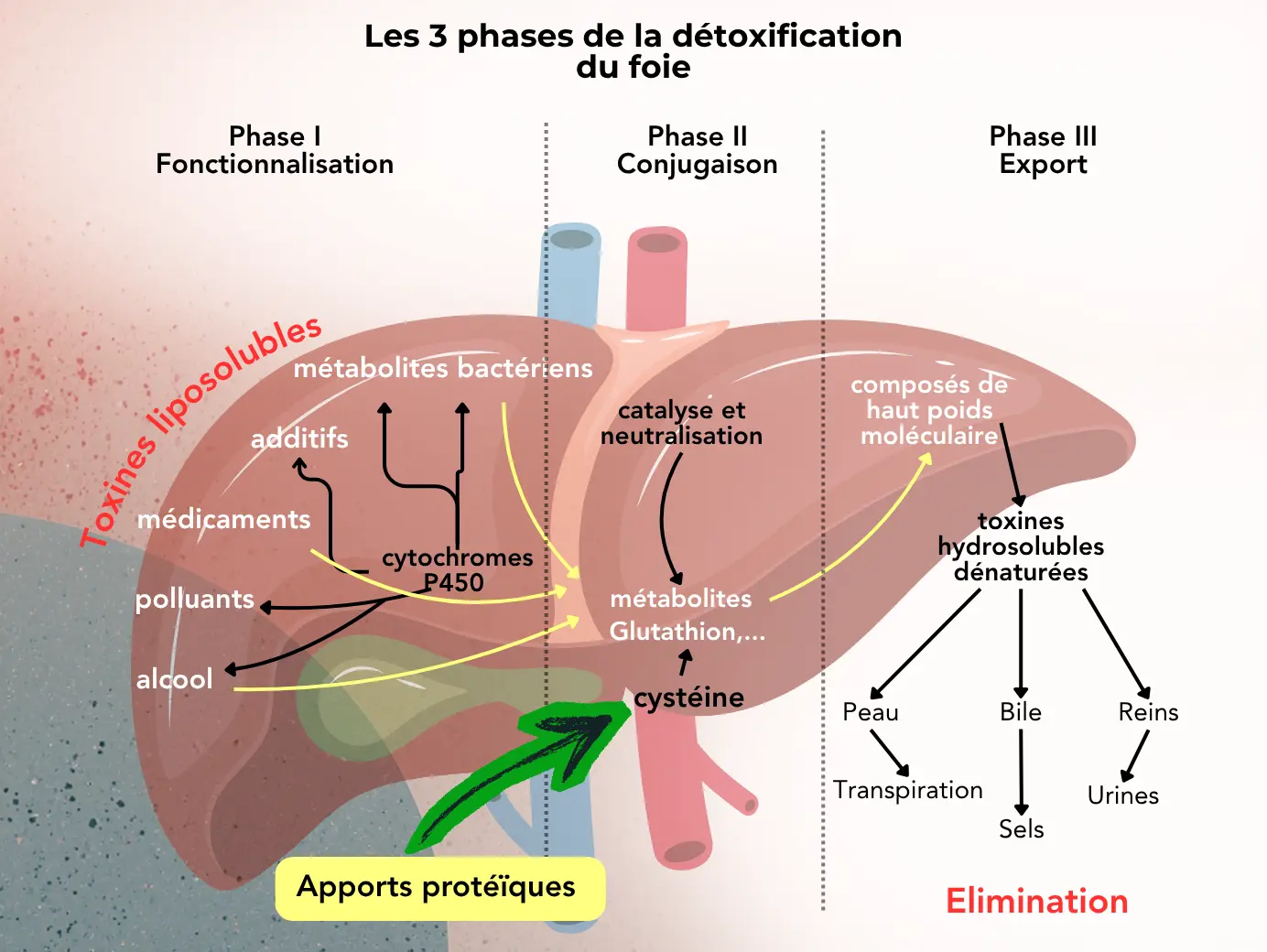
La biotransformation hépatique : un processus en trois phases
La biotransformation des xénobiotiques s’organise classiquement en trois phases fonctionnelles distinctes, dont la compréhension est essentielle pour évaluer l’impact potentiel de l’alimentation et comprendre la “détox du foie”.
Phase I : fonctionnalisation
Les enzymes de phase I, principalement les cytochromes P450 (CYP) — dont les isoformes CYP1A2, CYP2E1, CYP3A4 sont les plus représentés dans le foie humain — catalysent des réactions d’oxydation, de réduction ou d’hydrolyse, qui ont pour but de rendre soluble dans l’eau la molécule traitée. Ces réactions introduisent ou exposent des groupes fonctionnels polaires (–OH, –COOH, –NH₂) sur la molécule cible, la rendant plus réactive et, selon les cas, plus ou moins toxique.
C’est ici que se situe l’un des paradoxes majeurs de la détoxification : certains composés initialement inertes (pro-toxiques) peuvent être activés en métabolites réactifs potentiellement nocifs, par exemple mutagènes, lors de la phase I. C’est notamment le cas de certains hydrocarbures aromatiques polycycliques, du benzène ou de l’aflatoxine B1. Si la phase II ne suit pas suffisamment rapidement, ces intermédiaires réactifs peuvent s’accumuler et causer des dommages cellulaires.
Phase II : conjugaison
Les enzymes de phase II catalysent la conjugaison des métabolites issus de la phase I (ou directement de certains composés endogènes) à des groupements polaires : acide glucuronique (UDP-glucuronosyltransférases, UGT), sulfate (sulfotransférases, SULT), glutathion (glutathion S-transférases, GST), acétate, méthyle ou acides aminés (glycine, taurine).
Le résultat est un composé de haut poids moléculaire, encore plus fortement hydrosoluble, qui ne peut plus traverser les membranes biologiques, et qui sera exporté vers la bile ou les urines. La phase II est la phase clé de la neutralisation toxicologique.
Point biochimique critique : la conjugaison au glutathion (GSH) est l’une des plus importantes. Le glutathion est un tripeptide (γ-glutamyl-cystéinyl-glycine) dont la biosynthèse dépend directement de la disponibilité en cystéine — acide aminé semi-essentiel, limitant dans de nombreuses situations nutritionnelles déficitaires. C’est pourquoi un apport protéique suffisant conditionne directement l’efficacité de la phase II.
Phase III : export
Souvent méconnue, la phase III désigne l’action des transporteurs membranaires de la superfamille ABC (ATP-Binding Cassette), dont les membres les plus étudiés sont la P-glycoprotéine (P-gp, ABCB1), les protéines MRP (Multidrug Resistance-associated Proteins) et BCRP/ABCG2.
Ces transporteurs exportent activement les métabolites conjugués hors des cellules hépatiques vers la bile, ou hors des cellules intestinales vers la lumière digestive, prévenant leur réabsorption. Leur expression est inductible par certains composés phytochimiques, comme les polyphénols ou les isothiocyanates des crucifères.
Le rôle du microbiote intestinal dans la détoxification
Le microbiote intestinal constitue un acteur de plus en plus reconnu dans le métabolisme des xénobiotiques, au point que certains auteurs évoquent un « foie microbien » pour désigner l’ensemble des activités enzymatiques bactériennes impliquées dans la biotransformation.
Les bactéries intestinales expriment une large gamme d’enzymes hydrolytiques (β-glucuronidases, sulfatases, nitroréductases, azaoréductases) susceptibles de déconjuguer les métabolites liposolubles excrétés dans la bile, permettant leur réabsorption via le cycle entérohépatique. Ce mécanisme — bénéfique pour certaines molécules endogènes comme les acides biliaires ou certaines hormones — peut s’avérer délétère lorsqu’il s’applique à des xénobiotiques toxiques.
À l’inverse, certaines espèces bactériennes métabolisent des composés phytochimiques initialement peu biodisponibles en molécules actives et mieux biodisponibles (ex. : conversion des isoflavones de soja en équol, transformation des lignanes en entérolactone). La composition du microbiote constitue donc un facteur de variabilité interindividuelle majeur dans la réponse aux interventions nutritionnelles visant les voies de détoxification.
L’alimentation peut-elle moduler ces mécanismes ? Ce que dit la science
Les inducteurs naturels des enzymes de phase I et II
C’est probablement sur ce terrain que les données scientifiques sont les plus solides. Plusieurs familles de phytonutriments ont démontré, in vitro et dans des études animales, une capacité à moduler l’expression des enzymes de biotransformation — principalement via l’activation du facteur de transcription NRF2 (Nuclear Factor Erythroid 2-related factor 2), considéré comme le « maître régulateur » de la réponse antioxydante et de détoxification cellulaire.
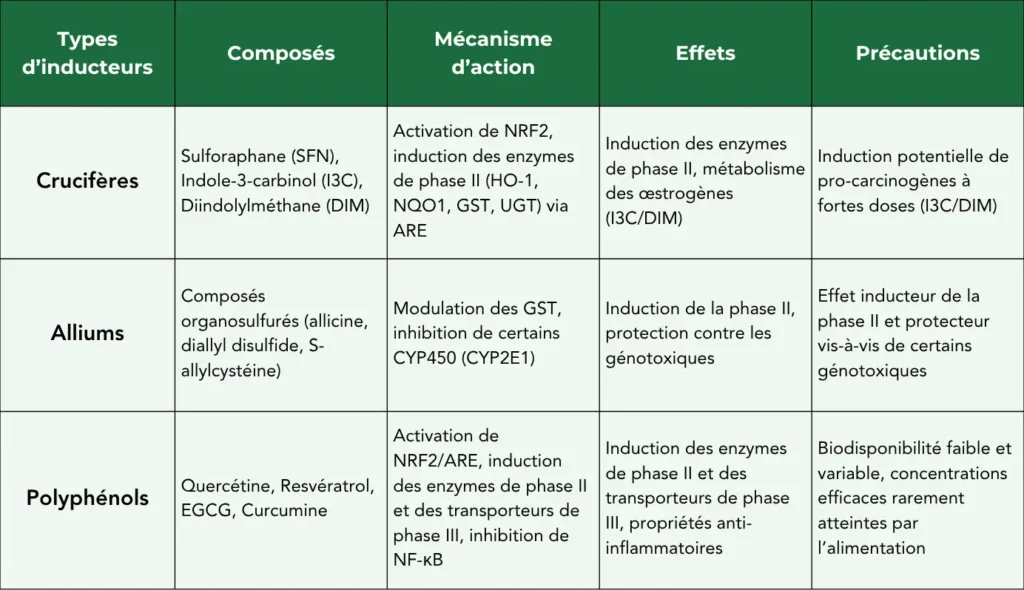
Les crucifères : isothiocyanates et indoles
Le sulforaphane (SFN) est l’isothiocyanate le mieux documenté. Issu de l’hydrolyse enzymatique (myrosinase) du glucoraphanine présent dans le brocoli, les choux de Bruxelles et le chou kale, il est un puissant inducteur de NRF2, entraînant l’expression des enzymes de phase II (HO-1, NQO1, GST, UGT) via les éléments de réponse antioxydante ARE (Antioxidant Response Elements) [1,2].
L’indole-3-carbinol (I3C) et son dimère le diindolylméthane (DIM) induisent préférentiellement les isoformes CYP1A1 et CYP1A2 des cytochromes P450, , ce qui explique par exemple leur intérêt théorique dans le métabolisme des œstrogènes (conversion vers la 2-hydroxyestrone, moins proliférative, au détriment de la 16α-hydroxyestrone) [3]. Toutefois, à fortes doses, cette induction peut également activer certains pro-cancérigènes, ce qui illustre la complexité des interactions phytochimiques-enzymes.
Les alliums : organosulfurés
L’ail (Allium sativum) et l’oignon contiennent des composés organosulfurés (allicine, diallyl disulfide, S-allylcystéine) qui modulent les glutathion-transférases et inhibent certains CYP450, notamment CYP2E1, impliqué dans l’activation métabolique de l’éthanol et des nitrosamines. Des études in vitro et chez le rongeur suggèrent un effet inducteur de la phase II et protecteur vis-à-vis de certains génotoxiques [4].
Les polyphénols : activation de NRF2
La quercétine (oignons, câpres, pommes), le resvératrol (raisin, myrtilles), l’EGCG (thé vert) et la curcumine (curcuma) activent tous la voie NRF2/ARE à des degrés divers, induisant les enzymes de phase II et les transporteurs de phase III. La curcumine est également inhibitrice de NF-κB, ce qui lui confère des propriétés anti-inflammatoires synergiques avec son effet de détoxification [5].
Il convient cependant d’être prudent dans le transfert de ces données à la pratique clinique : la biodisponibilité de ces composés est souvent faible et variable selon les individus, et les concentrations efficaces in vitro sont rarement atteintes par la seule alimentation.
| CE QUE DIT VRAIMENT LA RECHERCHE |
| Les études chez l’humain sont largement moins robustes que les études in vitro ou animales. |
| Les effets observés sont dose-dépendants, inductibles mais aussi inhibiteurs selon les concentrations (effet J inversé pour de nombreux polyphénols). |
| La biodisponibilité est un facteur limitant majeur : les isothiocyanates ont une excellente biodisponibilité, mais les polyphénols une biodisponibilité beaucoup plus variable (matrice alimentaire, microbiote, polymorphismes génétiques). |
| Les études d’intervention alimentaire de qualité (RCT avec biomarqueurs validés) restent rares. |
Les cofacteurs nutritionnels indispensables
Un angle souvent négligé dans la littérature de vulgarisation sur la « détox » est celui des cofacteurs nutritionnels. Les enzymes de biotransformation, comme toutes les enzymes, nécessitent des cofacteurs spécifiques dont la disponibilité conditionne directement leur activité.
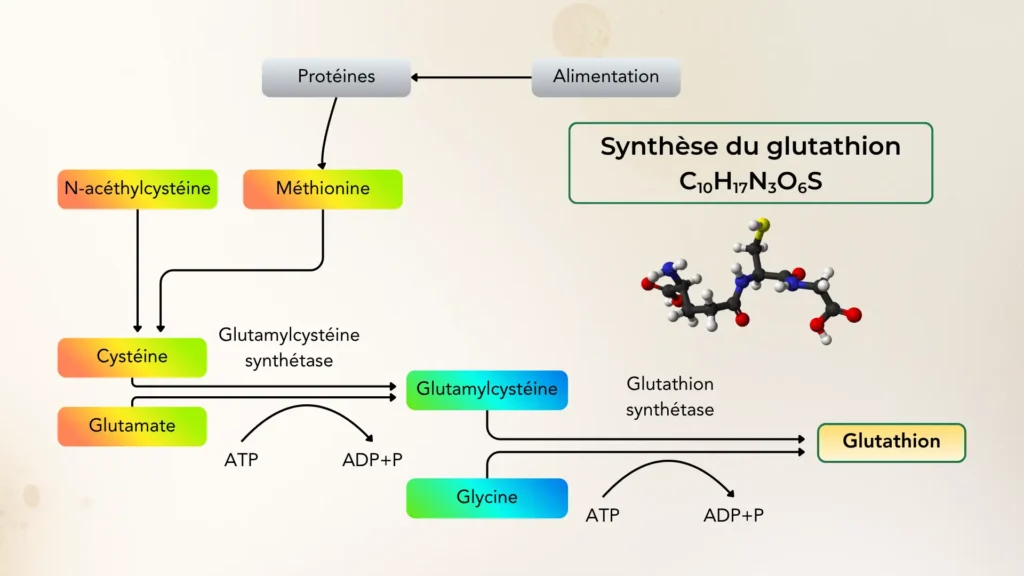
Le glutathion et ses précurseurs
Le glutathion (GSH) est le cofacteur de conjugaison le plus important du foie. Sa synthèse de novo dépend de trois acides aminés : glutamate, glycine et cystéine, ce dernier étant le facteur limitant. Tout régime restrictif en protéines (jeûne prolongé, mono-diète) peut paradoxalement réduire la capacité de conjugaison en phase II par appauvrissement du pool de cystéine disponible.
La N-acétylcystéine (NAC), précurseur direct du GSH, est utilisée cliniquement dans ce sens (traitement de l’intoxication au paracétamol).
Le sélénium est indispensable à la synthèse des sélénoprotéines, dont la glutathion peroxydase (GPx), enzyme clé de la neutralisation des peroxydes lipidiques.
Les vitamines du groupe B et la méthylation
Les réactions de méthylation constituent l’une des voies de conjugaison de phase II les plus importantes, notamment pour le métabolisme des métaux lourds (mercure, arsenic), des hormones stéroïdes et de nombreux xénobiotiques. Elles dépendent du cycle des folates et de la méthionine, impliquant les vitamines B2, B6, B12 et les folates comme cofacteurs. Un déficit en l’une de ces vitamines — fréquent en cas de régime restrictif ou de trouble de l’absorption — peut altérer significativement la capacité méthylante.
Le zinc, le magnésium et le soufre
Le zinc est un cofacteur de la superoxyde dismutase (Cu/Zn-SOD) et de nombreuses métalloenzymes impliquées dans la biotransformation. Le magnésium intervient comme cofacteur de plus de 300 enzymes, dont plusieurs impliquées dans la phosphorylation et la conjugaison. Les acides aminés soufrés (méthionine, cystéine, taurine) participent directement à la sulfatation en phase II et à la conjugaison à la taurine des acides biliaires.
Ce que l’alimentation ne peut pas faire
Il est essentiel d’énoncer clairement les limites biologiques de la « détox alimentaire ».
Premièrement, l’alimentation ne permet pas d’éliminer directement les toxines accumulées. Elle peut créer un contexte enzymatique favorable à leur biotransformation, mais la cinétique d’élimination des polluants organiques persistants (POPs), des métaux lourds bioaccumulés dans les tissus adipeux ou osseux, ou des dioxines, répond à des lois pharmacocinétiques qui ne sont pas modifiées par une cure de jus de raisin de trois jours. Les POPs, par définition lipophiles et résistants à la dégradation biologique, ont des demi-vies allant de plusieurs semaines à plusieurs décennies.
Deuxièmement, il n’existe pas de biomarqueur cliniquement validé permettant de mesurer l’effet « détox » d’une intervention alimentaire spécifique chez l’humain en bonne santé. Les marqueurs d’activité enzymatique hépatique (CYP450, GST) ne sont pas accessibles en routine, et les marqueurs indirects (capacité antioxydante totale du plasma, taux de glutathion érythrocytaire) sont influencés par de très nombreux facteurs confondants.
Troisièmement, les allégations de détoxification portant sur des organes spécifiques (« détox du foie », « drainage rénal ») n’ont aucune définition biochimique validée et constituent une simplification abusive de processus physiologiques extrêmement complexes.
Déconstruire les allégations commerciales
Les « cures détox » à l’épreuve des preuves
Une revue systématique publiée dans le Journal of Human Nutrition and Dietetics en 2015 par Klein et Kiat a analysé l’ensemble des études publiées sur les régimes détox commerciaux. Les auteurs ont conclu que les preuves de leur efficacité clinique étaient « largement insuffisantes », que les études disponibles souffraient de biais méthodologiques sévères (absence de groupe contrôle, effectifs réduits, absence de mesures objectives des « toxines ») et que le concept même de « détox alimentaire » manquait d’une définition consensuelle dans la littérature scientifique [6].
Ce constat reste valable en 2026 : malgré l’expansion du marché, le niveau de preuve n’a pas substantiellement progressé. La majorité des études positives sont financées par l’industrie des compléments alimentaires ou portent sur des populations cliniques spécifiques (insuffisance hépatique, intoxication médicamenteuse) qui ne sauraient être extrapolées à la population générale.
Le biais de définition
L’un des problèmes centraux est que le terme « détox » ne correspond à aucune entité biochimique définie. Selon les contextes, il peut désigner : l’élimination de résidus de pesticides, le soutien des enzymes hépatiques, la réduction du stress oxydatif, l’amélioration du transit intestinal, ou simplement une sensation subjective de « légèreté » et même parfois un sentiment euphorique de « nettoyage » purificateur. Cette polysémie rend toute évaluation scientifique rigoureuse quasi impossible.
Cas particuliers : certaines pratiques ont-elles un intérêt ?
Le jeûne et l’autophagie
Le jeûne — qu’il soit intermittent (16:8, 5:2) ou prolongé — induit l’autophagie, un processus de « recyclage » intracellulaire par lequel la cellule dégrade ses composants dysfonctionnels (protéines agrégées, mitochondries endommagées, agents pathogènes intracellulaires) via les lysosomes. Ce mécanisme, mis en lumière par les travaux de Yoshinori Ohsumi (prix Nobel 2016), a un réel fondement biologique et des implications cliniques potentielles dans la prévention des maladies neurodégénératives et du cancer [7].
Cependant, il est impératif de distinguer autophagie et « détoxification » au sens toxicologique du terme. L’autophagie ne concerne pas l’élimination des xénobiotiques exogènes : elle cible les composants cellulaires endogènes altérés. Assimiler les deux processus constitue une confusion conceptuelle courante dans la littérature de vulgarisation. Le jeûne ne constitue donc pas une réponse valable pour aider à une quelque « détoxification ».
L’hydratation et la fonction rénale
Une hydratation adéquate (1,5 à 2 L d’eau par jour dans les conditions habituelles) est absolument indispensable au bon fonctionnement de la filtration rénale et à l’excrétion urinaire des métabolites hydrosolubles. En ce sens, une augmentation de la consommation d’eau lors d’une période d’hydratation insuffisante chronique peut améliorer l’efficacité rénale d’élimination. Mais il n’existe aucune preuve que boire « plus que ses besoins » améliore les capacités de détoxification au-delà du niveau optimal.
Les fibres alimentaires et la recirculation entérohépatique
C’est l’un des mécanismes les mieux documentés sur le plan nutritionnel. Les fibres solubles (bêta-glucanes, pectines, inuline) et certains amidons résistants forment dans le côlon un gel qui piège les acides biliaires, les composés lipophiles conjugués excrétés dans la bile et certains xénobiotiques, limitant leur réabsorption et favorisant leur élimination fécale. C’est le principe pharmacologique de certaines résines échangeuses d’ions (cholestyramine) et il s’applique partiellement à certaines fibres alimentaires à haute capacité de liaison [8].
Les risques potentiels des protocoles « détox »
L’absence de bénéfice démontré ne suffit pas à disqualifier une pratique si elle est par ailleurs inoffensive. Mais certains protocoles « détox » présentent des risques réels qui méritent d’être signalés :
- Carences nutritionnelles : les cures hypocaloriques sévères ou les mono-diètes prolongées (plus de 3 à 5 jours) peuvent induire des déficits importants en protéines (avec réduction du pool de glutathion), en vitamines du groupe B, en zinc et en sélénium — précisément les cofacteurs dont dépend l’efficacité des voies de détoxification. Le résultat peut être paradoxalement une altération temporaire des capacités enzymatiques…. et une perte musculaire !
- Induction excessive de certains CYP450 : certains aliments ou compléments à forte dose peuvent soit stimuler ou inhiber des isoformes spécifiques de CYP450. Caféine, millepertuis, fortes doses d’I3C, hydrocarbures aromatiques issus de la cigarette ou d’aliments grillés au feu de bois sont par exemple des activateurs bien connus. A l’inverse, le jus de pamplemousse est un inhibiteur remarquable de plusieurs CYP. L’éthanol, lui, peut être soit inhibiteur soit activateur, selon la chronicité de l’exposition. Ces perturbateurs peuvent entraîner des interactions médicamenteuses cliniquement significatives chez les personnes ayant un traitement chronique [9]
- Perturbation du microbiote : des régimes très sélectifs ou des apports massifs en probiotiques non ciblés peuvent déstabiliser l’écosystème microbien intestinal, avec des effets imprévisibles sur le métabolisme des xénobiotiques.
- Effet de compensation comportementale : certains patients utilisent les cures détox comme « permission morale » de reprendre des comportements néfastes après la cure, annulant tout bénéfice potentiel.
Ce que l’on peut recommander en pratique
Une alimentation « support des voies de détoxification » : principes fondés sur les preuves
Si le concept marketing de « détox » ne résiste pas à l’examen scientifique, il n’en reste pas moins que l’alimentation exerce une influence réelle et significative sur l’efficacité des voies de biotransformation. Une approche nutritionnelle rationnelle peut être formulée autour des principes suivants :
Garantir un apport protéique suffisant
C’est le prérequis fondamental. Un apport de 0,8 à 1,2 g/kg/jour de protéines de haute valeur biologique (plus en cas d’activité physique intense ou de pathologie) assure la disponibilité en acides aminés précurseurs du glutathion (cystéine, glycine, glutamate), de la taurine et de la méthionine. Un régime végétalien mal planifié ou une restriction protéique prolongée peut compromettre cet apport.
Diversifier les apports végétaux
Une alimentation variée en végétaux fournit la gamme la plus large de composés phytonutriments modulateurs des enzymes de phase I et II. En pratique, cela se traduit par :
- 2 à 3 portions de crucifères par semaine (brocoli, chou, chou de Bruxelles, radis noir) pour les isothiocyanates
- Alliums quotidiens (ail, oignon, poireau, ciboulette) pour les organosulfurés
- Aromates frais et épices (romarin, thym, curcuma, gingembre) pour les polyphénols et terpènes
- Agrumes entiers (flavonoïdes, d-limonène) pour la modulation des CYP
- Thé vert (EGCG) et cacao non sucré (épicatéchine) sont des sources possibles de catéchines inductrices de NRF2
Réduire la charge toxique exogène
Soutenir les voies de détoxification sans simultanément réduire la charge en xénobiotiques revient à vider une baignoire avec le robinet ouvert. Les priorités pratiques sont : réduire l’exposition aux pesticides (privilégier les fruits et légumes de la liste « Dirty Dozen » en version bio), limiter la consommation d’alcool (inducteur puissant de CYP2E1, générateur de radicaux libres et consommateur de glutathion), éviter les aliments ultra-transformés riches en additifs, et choisir des contenants alimentaires adaptés (limitation de l’exposition aux phtalates et au bisphénol A).
L’importance de la fonction intestinale
L’intégrité de la barrière intestinale représente le premier rempart face aux xénobiotiques. Une perméabilité intestinale accrue (« leaky gut » ou intestin poreux) facilite le passage de lipopolysaccharides bactériens (LPS) et d’antigènes alimentaires dans la circulation portale, surchargeant secondairement le foie d’une charge inflammatoire et toxique supplémentaire.
Les stratégies nutritionnelles visant à renforcer cette barrière — apport adéquat en fibres prébiotiques (fructo-oligosaccharides, galacto-oligosaccharides, arabinoxylanes), en acides gras à chaîne courte (via la fermentation des fibres), en L-glutamine (carburant principal des entérocytes), en zinc et en vitamine D — s’inscrivent légitimement dans une approche de soutien aux voies de détoxification.
Perspectives : vers une approche individualisée
La recherche actuelle en pharmacogénomique nutritionnelle ouvre des perspectives fascinantes pour la personnalisation des recommandations. Les polymorphismes génétiques des enzymes de biotransformation — notamment les variants de CYP1A2, CYP2D6, GSTM1 (fréquemment délété dans la population générale), GSTT1 et MTHFR — induisent des variations interindividuelles considérables dans la réponse aux phytonutriments et dans l’efficacité des différentes voies de conjugaison [10].
À titre d’exemple, les individus homozygotes pour la délétion de GSTM1 (environ 50 % de la population caucasienne) ont une capacité réduite de conjugaison au glutathion et pourraient bénéficier davantage d’un apport accru en précurseurs du glutathion et en inducteurs de NRF2 que les individus possédant un allèle fonctionnel. Ces données, encore essentiellement issues d’études épidémiologiques et d’interventions de petit effectif, constituent la base de la nutrition de précision appliquée aux voies de détoxification.
Chez certaines personnes, les processus décrits plus hauts peuvent interférer avec d’autres voies métaboliques comme celle du soufre, par exemple, et une intervention via certains compléments alimentaires censés faciliter la « détoxification » peut alors se révéler être au contraire nocive. Dans tous les cas, une approche individualisée s’impose donc, à l’aide d’un professionnel de la nutrition maîtrisant ces aspects très complexes de notre fonctionnement.
| EN PRATIQUE — Recommandations concrètes |
| Prioriser un apport protéique suffisant avant toute autre intervention nutritionnelle. |
| Encourager une alimentation riche et diversifiée en végétaux, incluant régulièrement des crucifères et des alliums. |
| Réduire la charge toxique exogène (alcool, tabac, aliments ultra-transformés, pesticides) plutôt que de chercher à « compenser » a posteriori. |
| S’assurer d’une bonne hydratation (2-2,5 L/jour minimum) et d’un apport suffisant en fibres (25-30 g/jour). |
| Identifier les éventuels déficits en cofacteurs (vitamines B, zinc, sélénium, magnésium) avant de prescrire des compléments « détox ». |
Conclusion sur la détoxification (détox)
Le concept populaire de « détox alimentaire » repose sur un à priori biologiquement incorrect : l’organisme accumulerait passivement des « toxines » qu’il serait incapable d’éliminer sans l’aide d’une cure spécialisée. La réalité biochimique est à la fois plus complexe et plus rassurante : le corps humain dispose d’un système de biotransformation en trois phases, d’une remarquable efficacité, fonctionnant en continu dès la naissance.
La vitesse et l’efficacité de réactions chimiques impliquées est trèa variable d’une personne à l’autre. Ces variations individuelles sont dûes à l’âge, au sexe, aux maladies et à leurs traitements médicamenteux, au régime alimentaire, au mode de vie (tabac, alcool, …) et bien sûr au contrôle génétique. Il serait donc inexact de conclure que l’alimentation est sans effet sur ces voies. La science apporte des preuves croissantes — bien qu’encore incomplètes sur le plan des études d’intervention humaine — que certains phytonutriments (isothiocyanates, polyphénols, organosulfurés) peuvent moduler l’expression des enzymes de phase I et II via des voies de signalisation cellulaire identifiées (NRF2/ARE en tête). De même, les cofacteurs nutritionnels (glutathion, vitamines B, zinc, sélénium) sont des déterminants directs de la capacité enzymatique de conjugaison.
La ligne de démarcation entre ce qui est scientifiquement fondé et ce qui relève du marketing est donc claire : l’alimentation peut soutenir les voies de détoxification physiologiques, à condition d’être suffisante en protéines, diversifiée en végétaux et pauvre en charge toxique exogène. Elle ne peut ni remplacer ces voies, ni éliminer des polluants bioaccumulés, ni compenser en 72 heures des années d’exposition. Il s’agit de sortir du registre de la magie pour entrer dans celui de la biochimie nutritionnelle appliquée. Les simplifications marketing utilisées pour vendre des protocoles de cures miraculeuses censées « nettoyer » et « purifier » sont à éviter soigneusement : notre organisme n’est pas un carburateur qui s’encrasse avec le temps. En résumé, il n’y a pas de recette détox.
Quelques références
| Auteurs et Titres | Journal et Détails | Lien |
| Zhang Y, Talalay P. Anticarcinogenic activities of organic isothiocyanates: chemistry and mechanisms. | Cancer Res. 1994;54(7 Suppl):1976s-1981s. | Accès |
| Bradlow HL, et al. 2-Hydroxyestrone: the ‘good’ estrogen. | J Endocrinol. 1996;150 Suppl:S259-265. | Accès |
| Klein AV, Kiat H. Detox diets for toxin elimination and weight management: a critical review of the evidence. | J Hum Nutr Diet. 2015;28(6):675-686. | Accès |


