La fatigue chronique n’est pas une fatalité. Vous souffrez d’une fatigue qui ne cède pas au repos. Ce n’est pas dans votre tête mais dans vos cellules.
Contenu de l'article
ToggleDéfinition de la fatigue chronique
La fatigue chronique est l’un des motifs de consultation les plus fréquents en médecine générale, et pourtant l’un des plus mal compris. Derrière ce terme aux contours flous se cachent des réalités biologiques profondément différentes : une fatigue physiologique, normale et réparatrice, une fatigue chronique fonctionnelle qui s’installe insidieusement sur fond de mode de vie dégradé, et enfin une entité clinique à part entière, l’Encéphalomyélite Myalgique / Syndrome de Fatigue Chronique (EM-SFC), dont la reconnaissance scientifique internationale ne cesse de s’affiner depuis le rapport fondateur de l’Institute of Medicine en 2015.
Ce que ces trois formes ont en commun, c’est qu’elles impliquent toutes, à des degrés divers, des dérèglements biochimiques profonds — au niveau cellulaire, immunitaire, neuroendocrinien et digestif. Et c’est précisément là que la nutrition intervient : non pas comme un adjuvant ou un « plus », mais comme un levier thérapeutique de première ligne, capable d’agir sur les causes en amont des symptômes.
Cet article propose une lecture intégrative et mécanistique de la fatigue chronique, structurée autour de trois axes biochimiques majeurs : la dysfonction mitochondriale, les carences en micronutriments, et l’implication du microbiote intestinal. L’objectif est double — offrir aux professionnels de santé un cadre rigoureux, et donner aux patients des clés de compréhension concrètes pour agir sur leur alimentation avec pertinence.
De la fatigue banale à l’EM-SFC : un continuum clinique à hiérarchiser
Trois tableaux cliniques, trois réalités biologiques
La fatigue physiologique est une réponse normale de l’organisme à un effort physique ou intellectuel soutenu. Elle est normalement transitoire, proportionnelle à la sollicitation, et disparaît après une nuit de sommeil réparateur. Sa résolution ne pose aucun problème diagnostique.
La fatigue chronique non spécifique, en revanche, s’installe sur plusieurs semaines à plusieurs mois, sans cause évidente. Elle touche une proportion croissante de la population, souvent sur fond de stress chronique, de déséquilibres alimentaires, de perméabilité intestinale augmentée ou de carences en micronutriments. Elle ne répond pas au repos seul et nécessite une investigation clinique et biologique approfondie.
L’EM-SFC, enfin, est une maladie systémique invalidante, caractérisée par une fatigue profonde et non soulagée par le repos, une intolérance à l’effort (malaise post-effort PEM — Post-Exertional Malaise), des troubles cognitifs sévères (brouillard mental, ou “brain fog”), et des dysfonctions autonomiques (atteignant le système nerveux autonome). Elle touche environ 0,4 % de la population mondiale, soit plusieurs dizaines de milliers de personnes en France, et reste dramatiquement sous-diagnostiquée.
L’intérêt d’inclure l’EM-SFC dans cette analyse est scientifique : elle constitue un modèle extrême qui révèle, avec une clarté rare, les mécanismes biochimiques sous-jacents à toutes les formes de fatigue chronique. Ce que l’on observe à l’état amplifié dans l’EM-SFC se retrouve, atténué, dans les formes plus courantes.
Tableau comparatif des trois formes de fatigue
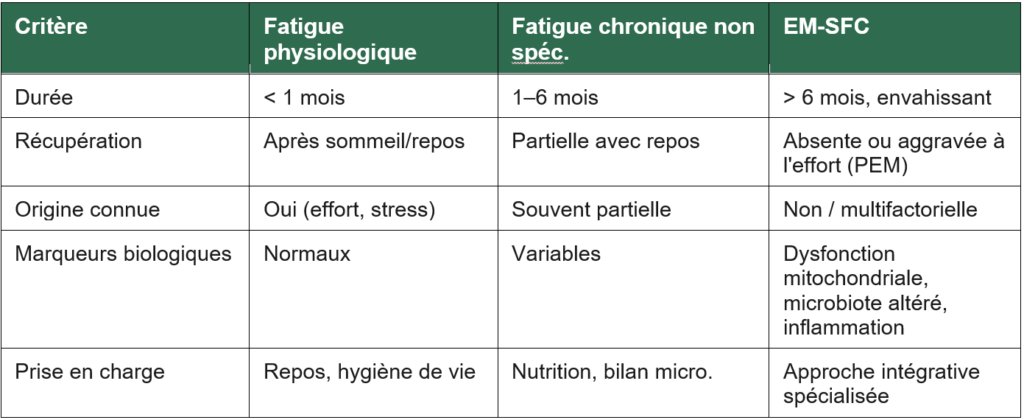
L’EM-SFC n’est pas une maladie psychosomatique
Il faut insister sur ce point, car il conditionne la prise en charge nutritionnelle. Pendant des décennies, la fatigue chronique sévère a été renvoyée au champ psychiatrique, faute de marqueurs biologiques identifiés. Les travaux récents — notamment ceux de Robert Naviaux sur la métabolomique (PNAS, 2016), de Fluge et Mella sur les autoanticorps, et les données post-COVID — ont radicalement changé la donne. L’EM-SFC est désormais reconnue comme une maladie neuroimmune à substrat biochimique mesurable. Cette réhabilitation scientifique ouvre la voie à des interventions nutritionnelles ciblées, fondées sur des mécanismes identifiés.
L’axe mitochondrial : quand la cellule perd le fil de l’énergie
Un rappel fondateur : comment la cellule fabrique son énergie
Toute cellule vivante, quelle que soit son type et son rôle biologique, dépend de l’adénosine triphosphate (ATP) pour fonctionner — que ce soit pour contracter un muscle, transmettre un signal nerveux, sécréter une hormone, ou tout simplement synthétiser une protéine. L’ATP est produite principalement dans les mitochondries, ces organites appelés à juste titre « centrales énergétiques de la cellule ». Le processus passe par trois grandes étapes : la glycolyse (dans le cytoplasme) et l’oxydation des acides gras (appelée β-oxydation), le cycle de Krebs (dans la matrice mitochondriale), et la chaîne de transport des électrons couplée à l’ATP synthase (sur la membrane interne mitochondriale). Ce dernier mécanisme, la phosphorylation oxydative, génère environ 90 % de l’énergie cellulaire totale.
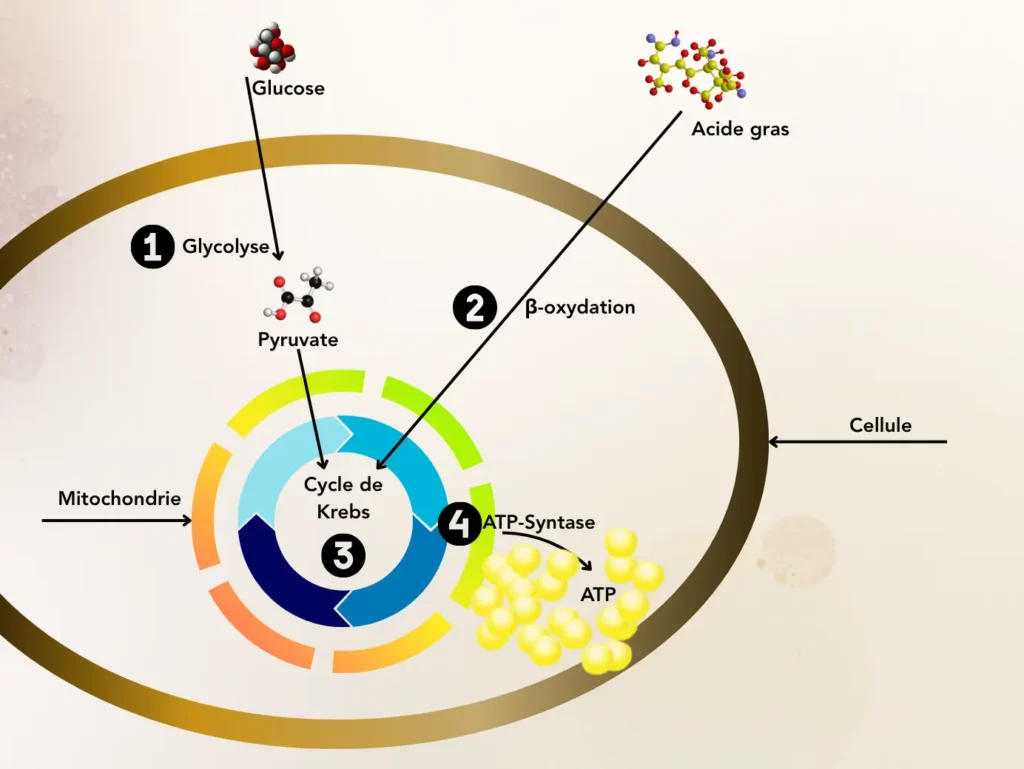
Ce schéma, enseigné en biochimie fondamentale, prend une résonance clinique toute particulière lorsqu’on comprend que n’importe quelle perturbation à l’un de ces niveaux — qu’elle soit d’ordre nutritionnel, inflammatoire, ou oxydatif — peut compromettre la production d’ATP et se traduire, à l’échelle de l’organisme, par une fatigue profonde et persistante.
Ce type de perturbations intervient au niveau de tout type de cellule : celles des muscles squelettiques, du muscle cardiaque, du tissu nerveux, du système digestif, des glandes hormonales… Ceci explique que la fatigue physique et la faiblesse musculaire s’accompagnent souvent, en cas de fatigue chronique, d’une fonction cardiaque altérée, de troubles digestifs et de brouillard mental. Ceci est d’autant plus marqué quand une alimentation déficiente s’ajoute à cette condition.
Dysfonction mitochondriale : les preuves s’accumulent
Dans la fatigue chronique, et de façon particulièrement documentée dans l’EM-SFC, plusieurs anomalies mitochondriales ont été mises en évidence. Les travaux de Naviaux et al. (2016), utilisant la métabolomique non ciblée, ont identifié un profil métabolique caractéristique rappelant une réponse de défense cellulaire archaïque : la diapausa — une mise en veille métabolique qui réduit l’activité mitochondriale et l’utilisation de l’oxygène.
Des altérations des complexes de la chaîne respiratoire (notamment les complexes I et III) ont été observées, accompagnées d’une surproduction d’espèces réactives de l’oxygène (ROS). Ce stress oxydatif provoque une altération des protéines et de l’ADN mitochondrial, ainsi qu’une peroxydation lipidique des membranes mitochondriales, altérant leur perméabilité et leur capacité à maintenir le gradient de protons nécessaire à la synthèse d’ATP. On observe également un découplage partiel de l’ATP synthase, c’est-à-dire une dissipation de l’énergie en chaleur plutôt qu’en ATP utile.
Parallèlement, des études ont montré une déplétion en certains cofacteurs essentiels à la chaîne respiratoire, notamment la coenzyme Q10 (CoQ10) et la L-carnitine, dont les taux plasmatiques sont significativement abaissés chez de nombreux patients souffrant de fatigue chronique sévère.
Le “metabolic switch” altéré : implications nutritionnelles directes
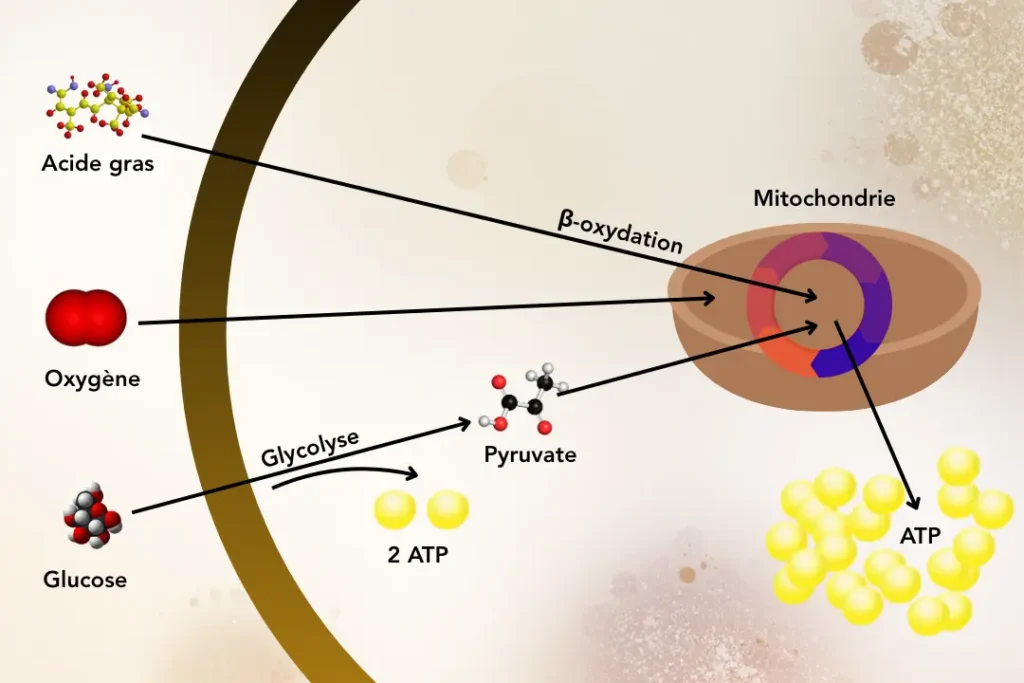
L’organisme sain dispose d’une flexibilité métabolique remarquable : il peut passer de l’utilisation du glucose (glycolyse) à celle des acides gras (β-oxydation) selon les besoins, les disponibilités énergétiques, ainsi que l’état nutritionnel et le degré d’inflammation. Ce «metabolic switch» est finement régulé et dépend, entre autres, de la signalisation insulinique, des réserves de glycogène, et de l’intégrité des transporteurs mitochondriaux d’acides gras. Il n’est d’ailleurs que partiel, l’oxydation des acides gras nécessitant un métabolite du glucose pour fonctionner à son plein rendement. Et surtout, il dépend de la bonne santé des mitochondries, et de leur capacité à transformer pyruvate et acides gras en molécules d’ATP.
Dans la fatigue chronique, cette flexibilité est altérée. La cellule reste « bloquée » en mode glycolytique, incapable de basculer efficacement vers la β-oxydation, qui est dépendante d’une activité mitochondriale correcte. La conséquence pratique est double : une dépendance accrue aux glucides rapides (dont la consommation peut donner l’illusion d’un regain d’énergie tout en entretenant le cercle vicieux), et une incapacité à tirer parti des réserves lipidiques comme source d’énergie stable, celle qui est pourtant la plus efficace en termes de rendement énergétique. Dans ces conditions, la fabrication d’ATP est trop lente et devient insuffisante. De plus, le faible rendement énergétique du glucose peut provoquer une perte importante en base purique adénine précurseur de l’ATP, empêchant la réserve d’énergie de se reconstituer, et instaurant une spirale délétère pour le fonctionnement cellulaire. Ces données ont des implications directes sur la composition de l’alimentation recommandée, sur laquelle nous reviendrons.
Les cofacteurs nutritionnels de la mitochondrie
La mitochondrie est une machine biochimique extraordinairement dépendante de micronutriments précis. Le CoQ10 (ubiquinone) est indispensable au transfert des électrons entre les complexes I/II et le complexe III ; son déficit ralentit l’ensemble de la chaîne. La L-carnitine transporte les acides gras à longue chaîne à travers la membrane mitochondriale interne — sans elle, les lipides ne peuvent être oxydés. Le NAD⁺ et ses précurseurs (nicotinamide riboside, NMN) sont des cofacteurs centraux des complexes I et III et jouent un rôle dans la réparation de l’ADN mitochondrial, dont les dommages s’accumulent sous l’effet du stress oxydatif.
L’acide alpha-lipoïque mérite également une mention particulière : antioxydant liposoluble et hydrosoluble à la fois, il régénère le glutathion, la vitamine C et la vitamine E au sein même de la mitochondrie. Sa supplémentation a montré des effets favorables sur les marqueurs de stress oxydatif dans plusieurs études cliniques.
| Point pratique — Soutenir la biogenèse mitochondriale par l’alimentation Des composés phytochimiques comme le resvératrol (raisins, vin rouge) et la quercétine (câpres, oignons, pommes) activent la voie PGC-1α, facteur de transcription maître de la biogenèse mitochondriale. Les oméga-3 à longue chaîne (EPA/DHA) améliorent la fluidité membranaire mitochondriale. Une alimentation à faible charge glycémique favorise le metabolic switch et réduit la surproduction de ROS liée aux pics de glucose. Ces données ne remplacent pas une supplémentation ciblée mais renforcent son efficacité. |
Les micronutriments sentinelles : des déficits silencieux aux conséquences profondes
L’un des aspects les plus sous-estimés de la fatigue chronique est la prévalence des déficits subcliniques en micronutriments — c’est-à-dire des carences qui n’atteignent pas le seuil pathologique défini par les normes biologiques standard, mais qui compromettent néanmoins de nombreuses voies métaboliques. Il est essentiel de comprendre que les valeurs de référence des laboratoires sont établies pour détecter les maladies carentielles, non pour optimiser la fonction cellulaire. Le praticien averti doit raisonner en termes de seuils optimaux, non de seuils pathologiques.
Fer et ferritine : au-delà de l’anémie
Le fer est souvent uniquement associé à l’anémie dans l’imaginaire collectif. C’est réducteur. Il est indispensable au bon fonctionnement des complexes I à III de la chaîne respiratoire mitochondriale (via les centres fer-soufre), à la synthèse de neurotransmetteurs comme la dopamine et la sérotonine (il est cofacteur de la tyrosine hydroxylase et de la tryptophane hydroxylase), ainsi qu’à la myélinisation des fibres nerveuses. Une ferritine inférieure à 50 µg/L — valeur souvent considérée comme « normale » par les laboratoires — peut s’accompagner d’une fatigue significative et de troubles cognitifs, en l’absence de toute anémie. Ce point est capital en pratique clinique.
Magnésium : le grand oublié
Le magnésium est cofacteur de plus de 300 réactions enzymatiques dans l’organisme, dont la quasi-totalité des réactions impliquant l’ATP (qui existe biologiquement sous forme de complexe Mg-ATP). Il est donc fondamental à la bioénergétique cellulaire. Il joue également un rôle central dans la régulation de l’axe hypothalamo-hypophyso-surrénalien (HPA) et dans la transmission neuromusculaire. Son déficit subclinique est quasi-universel dans les sociétés occidentales, du fait de l’appauvrissement des sols, du raffinage alimentaire, de la consommation excessive de produits ultra-transformés et du stress chronique qui favorise sa fuite de l’organisme. Le dosage plasmatique standard sous-estime chroniquement le déficit intracellulaire — préférer le dosage érythrocytaire ou l’évaluation clinique combinée.
Vitamines du groupe B : les chefs d’orchestre du métabolisme énergétique
Les vitamines B forment un groupe indissociable dans leur action sur la bioénergétique. La thiamine (B1) est un des coenzymes de la pyruvate déshydrogénase, enzyme-clé permettant l’entrée du pyruvate dans le cycle de Krebs ; une carence ralentit directement la production d’ATP et se manifeste notamment par une fatigue neurologique. La riboflavine (B2) et la niacine (B3) sont les précurseurs respectifs de la FAD et du NAD⁺/NADH, coenzymes indispensables aux complexes I et II de la chaîne respiratoire — leur déficit est directement pro-fatigue.
Les vitamines B6, B9 et B12 agissent en synergie dans le cycle de la méthylation, processus épigénétique essentiel à la synthèse de neurotransmetteurs, à la réparation de l’ADN et à la régulation de l’homocystéine. Une hyperhomocystéinémie, fréquente en cas de déficit en B9 ou B12, est associée à une inflammation vasculaire de bas grade et à des troubles cognitifs. Il convient de noter que la forme méthylée de la B12 (méthylcobalamine) est à privilégier en supplémentation, notamment chez les porteurs du polymorphisme MTHFR.
Vitamine D, zinc, sélénium : des acteurs immunométaboliques
La vitamine D agit bien au-delà du métabolisme osseux. Ses récepteurs (VDR) sont présents sur pratiquement toutes les cellules du système immunitaire, et son rôle dans la modulation de la réponse inflammatoire est désormais bien documenté. Une carence en vitamine D est associée à une fatigue neuromusculaire, une sensibilité accrue aux infections et une dysrégulation immunitaire — terrain propice à l’entretien d’une inflammation chronique de bas grade. En pratique, un taux de 25-OH-D3 inférieur à 40 ng/mL justifie une supplémentation, associée à la vitamine K2 pour optimiser l’utilisation du calcium.
Le zinc et le sélénium sont des cofacteurs essentiels des superoxyde dismutases (SOD), enzymes antioxydantes majeures, et de la glutathion peroxydase pour le sélénium. Leur déficit aggrave le stress oxydatif mitochondrial. Par ailleurs, l’iode et le sélénium sont tous deux indispensables à la synthèse et à l’activation des hormones thyroïdiennes — une hypothyroïdie infraclinique étant une cause fréquente et sous-diagnostiquée de fatigue chronique.
L’axe intestin-cerveau-mitochondrie : le microbiote au cœur de la fatigue
Dysbiose et fatigue chronique : l’émergence d’un lien causal
La recherche sur le microbiote intestinal dans la fatigue chronique a connu une véritable accélération au cours de la dernière décennie. Les travaux de Giloteaux et al. (Microbiome, 2016) ont montré, chez des patients EM-SFC, une réduction significative de la diversité microbienne et une diminution des espèces productrices de butyrate — notamment Faecalibacterium prausnitzii et Roseburia intestinalis — avec en parallèle un enrichissement en espèces pro-inflammatoires. Ces altérations ne sont pas anodines ; elles ont des répercussions systémiques directes sur la bioénergétique, le système immunitaire et le cerveau. Des travaux plus récents, notamment en lien avec les séquelles post-COVID (ou “long COVID”), ont confirmé et étendu ces observations, suggérant que la dysbiose pourrait être à la fois une cause et une conséquence de la fatigue chronique — créant un cercle vicieux auto-entretenu que l’alimentation peut contribuer à briser.
Les métabolites microbiens comme acteurs biochimiques
Le microbiote intestinal ne se contente pas de digérer les fibres alimentaires : il produit une pharmacopée de métabolites bioactifs dont certains influencent directement la fatigue. Les acides gras à chaîne courte (SCFA) — acétate, propionate et surtout butyrate — sont les produits de fermentation bactérienne des fibres alimentaires. Le butyrate est la principale source d’énergie des colonocytes, mais il est également un puissant modulateur épigénétique (inhibiteur des histones désacétylases) et un régulateur de la perméabilité de la barrière intestinale.
Un aspect particulièrement intéressant est le lien entre microbiote et métabolisme du tryptophane, précurseur de la sérotonine (voie TPH1/TPH2) mais aussi, en cas d’inflammation, de la kynurénine via l’enzyme IDO-1 (indoléamine 2,3-dioxygénase). L’activation de la voie kynurénine au détriment de la voie sérotonine est associée à la fatigue, à la dépression et aux troubles cognitifs. Or, cette bascule est directement modulée par l’état inflammatoire — lui-même influencé par le microbiote. La boucle est bouclée.
L’hyperperméabilité intestinale : amplificateur systémique de la fatigue
La barrière intestinale est constituée d’une couche unicellulaire de cellules épithéliales reliées par des jonctions serrées (tight junctions) — des complexes protéiques incluant la claudine, l’occludine et les protéines ZO. En cas de dysbiose, de stress chronique, d’alimentation pro-inflammatoire ou de déficit en zinc et en glutamine, ces jonctions s’altèrent. La perméabilité intestinale augmente, permettant le passage de fragments bactériens — notamment les lipopolysaccharides (LPS) — dans la circulation sanguine.
Cette endotoxémie métabolique « silencieuse » active les récepteurs TLR4 (Toll-Like Receptor 4) des cellules immunitaires et des cellules microgliales cérébrales, déclenchant une cascade inflammatoire à bas bruit mais chronique. Les cytokines pro-inflammatoires produites (IL-1β, IL-6, TNF-α) traversent la barrière hémato-encéphalique ou signalent directement via le nerf vague, induisant le syndrome appelé «sickness behavior» — fatigue, retrait social, altérations cognitives — qui n’est pas une pathologie en soi mais une réponse immunitaire adaptative devenue délétère lorsqu’elle se chronicise.
La connexion microbiote-mitochondries
Un lien direct, encore émergent mais déjà solidement documenté, unit le microbiote aux mitochondries. D’une part, les SCFA produits par les bactéries — en particulier le butyrate — modulent directement la biogenèse mitochondriale et réduisent le stress oxydatif dans les cellules épithéliales. D’autre part, l’inflammation intestinale chronique induite par la dysbiose génère, outre un manque de butyrate, un stress oxydatif systémique qui atteint les mitochondries de toutes les cellules de l’organisme, aggravant les déficits de production d’ATP.
Autrement dit, prendre soin de son microbiote n’est pas seulement une affaire digestive : c’est une manière directe de protéger et de soutenir la fonction mitochondriale, et par extension, de lutter contre la fatigue chronique à sa source.
Leviers nutritionnels sur le microbiote
Les données cliniques convergent aujourd’hui pour identifier plusieurs axes d’intervention alimentaire sur le microbiote. Les fibres fermentescibles — inuline, fructo-oligosaccharides (FOS), galacto-oligosaccharides (GOS), amidon résistant — constituent le substrat privilégié des bactéries productrices de butyrate. Leur consommation régulière, progressive pour éviter les inconforts digestifs, est l’un des leviers les plus puissants disponibles.
Les aliments fermentés — kéfir, yaourt, choucroute, kimchi, kombucha — ont montré dans une étude randomisée contrôlée publiée dans Cell (Sonnenburg et al., 2021) un effet significatif sur la diversité microbienne et la réduction des marqueurs inflammatoires, supérieur à celui d’un régime riche en fibres seul. Cette découverte renouvelle l’intérêt clinique pour la fermentation alimentaire traditionnelle.
Concernant les probiotiques, les données restent hétérogènes dans la fatigue chronique, en raison de la variabilité des souches, des doses et des populations étudiées. Les espèces Lactobacillus acidophilus, Bifidobacterium longum et Lactobacillus rhamnosus GG montrent les profils les plus prometteurs. Une supplémentation probiotique ciblée doit être individualisée et ne saurait se substituer à une réforme alimentaire de fond.
| Point pratique — Alimentation et microbiote anti-fatigue Privilégier les végétaux diversifiés (30 espèces végétales différentes par semaine est un objectif validé par la recherche), les céréales complètes, les légumineuses et les oléagineux comme substrats prébiotiques. Intégrer quotidiennement un à deux aliments fermentés de qualité. Éliminer les perturbateurs du microbiote : sucres raffinés, alcool, émulsifiants alimentaires (polysorbate 80, carraghénanes), édulcorants de synthèse. En cas de symptômes digestifs associés, un protocole FODMAP, seulement à court terme, peut être envisagé avant réintroduction progressive |
L’axe neuroendocrinien et l’inflammation de bas grade
L’axe HPA et la fatigue : nuances nécessaires
L’axe hypothalamo-hypophyso-surrénalien (HPA) est le système central de régulation du stress. En situation de stress chronique — physique ou psychologique — il peut être hyper- ou hypo-activé, perturbant la sécrétion de cortisol selon un rythme circadien normalement bien défini. Un aplatissement de la courbe diurne du cortisol, avec un taux matinal bas et un pic atténué, est fréquemment observé dans la fatigue chronique sévère.
Il convient ici d’être rigoureux sur le concept de «fatigue surrénalienne», très répandu dans la littérature grand public mais mal défini scientifiquement. Ce terme recouvre une réalité biologique réelle — la dérégulation de l’axe HPA — mais ne doit pas être confondu avec une insuffisance surrénalienne vraie, qui est une pathologie endocrinienne distincte. La nuance est importante pour éviter des supplémentations inadaptées en cortisol ou en DHEA.
Inflammation chronique de bas grade : le sickness behavior comme clé de compréhension
L’inflammation chronique de bas grade est un état dans lequel le système immunitaire reste activé à un niveau modéré mais persistant, produisant en continu des cytokines pro-inflammatoires — interleukine-6 (IL-6), interleukine-1β et TNF-α — sans déclencher les signes classiques de l’inflammation aiguë (fièvre, rougeur, chaleur). Cet état est directement relié à la fatigue via le «sickness behavior» : un ensemble de comportements adaptatifs — fatigue, retrait, hypersomnie, anorexie — qui constituent une réponse immunitaire normale mais qui, lorsqu’ils se chronicisent, deviennent profondément invalidants.
L’Indice Inflammatoire Alimentaire (DII — Dietary Inflammatory Index), développé par Shivappa et al. (2014), est un outil clinique proposant de scorer le pouvoir pro- ou anti-inflammatoire du régime alimentaire d’un individu à partir de 45 paramètres nutritionnels. Des scores DII élevés (régime pro-inflammatoire) sont significativement associés à une fatigue perçue plus intense dans plusieurs études de cohorte. Cet outil offre une base objective pour prioriser les changements alimentaires.
Chrononutrition : le timing comme variable thérapeutique
La chrononutrition est un champ en plein essor qui étudie l’interaction entre les rythmes circadiens et le métabolisme nutritionnel. Les mitochondries ont leur propre horloge biologique, synchronisée avec le rythme veille/sommeil. Des repas décalés, sautés ou pris irrégulièrement perturbent cette synchronisation et altèrent l’efficacité de la phosphorylation oxydative. En pratique, un petit-déjeuner riche en protéines et en bonnes graisses — pris dans les deux heures suivant le réveil — amorce efficacement le metabolic switch et stabilise la glycémie sur l’ensemble de la journée, limitant les à-coups énergétiques qui amplifient la fatigue.
Recommandations nutritionnelles intégratives : de la théorie à la pratique
Construire une alimentation bioénergétique
L’assiette qui soutient la mitochondrie et le microbiote n’est pas une assiette de restriction — c’est une assiette de densité micronutritionnelle. Elle se construit autour de végétaux diversifiés et colorés (source de polyphénols, fibres et antioxydants), de protéines de qualité (pour fournir les acides aminés précurseurs des neurotransmetteurs et du glutathion) et en quantité suffisante, de bonnes graisses (oméga-3, huiles vierges de première pression à froid, oléagineux) et de glucides complexes à faible index glycémique. Elle exclut les produits ultra-transformés, les sucres raffinés et l’alcool — trois perturbateurs mitochondriaux et microbiotiques majeurs. De plus, l’équilibre quantitatif de tous ces nutriments est essentiel, c’est le levier d’action le plus efficace sur la santé mitochondriale.
La supplémentation ciblée : une individualisation indispensable
Aucune supplémentation ne peut être recommandée de façon universelle en dehors d’un bilan biologique et global préalable. La hiérarchie des priorités est à établir selon le profil de chaque patient. Les candidats les plus fréquents à la supplémentation dans les contextes de fatigue chronique sont le magnésium sous forme hautement biodisponible (bisglycinate, malate), la vitamine D3 associée à la K2, la vitamine B12 méthylée et la B9 sous forme de méthylfolate, le CoQ10 sous forme d’ubiquinol, et la L-carnitine. Le fer héminique issu de l’alimentation reste supérieur aux suppléments ferreux en termes de tolérance digestive, mais une supplémentation peut s’avérer nécessaire en cas de carence documentée.
D’autres compléments ont un intérêt en prise ponctuelle, et ne doivent être pris que sous la supervision d’un professionnel de santé formé à leur utilisation.
Ce que la science ne valide pas
L’honnêteté intellectuelle impose de mentionner les approches dont les données sont encore insuffisantes ou contradictoires. Le jeûne prolongé, très populaire, est contre-indiqué dans les formes sévères d’EM-SFC : l’intolérance à l’effort (avec malaise post-effort) s’applique également au stress métabolique du jeûne prolongé, qui peut déclencher des rechutes. La privation de macronutriments énergétiques ne peut au contraire qu’amplifier un état et un fonctionnement déjà dégradés. La diète cétogène pourrait en théorie contourner le défaut de metabolic switch. Etant très dépendante de l’état mitochondrial, elle n’est justement pas un bon candidat pour rétablir un fonctionnement correct des voies énergétiques. Elle fait l’objet d’études préliminaires mais sans essais randomisés contrôlés suffisants à ce jour. Elle a de plus de nombreux inconvénients à moyen et long terme.
Conclusion sur la fatigue chronique
La fatigue chronique n’est pas une fatalité, ni une plainte subjective sans substrat biologique. C’est un signal d’alarme biochimique multisystémique qui nous parle de mitochondries épuisées, de micronutriments manquants, d’un microbiote appauvri et d’une inflammation entretenue en silence. Ces mécanismes s’alimentent mutuellement, formant des cercles vicieux que seule une intervention intégrée peut véritablement interrompre.
La nutrition occupe dans ce contexte une place de premier plan, non pas comme support accessoire, mais comme outil thérapeutique à part entière. Elle agit en amont, sur les causes — et non sur les symptômes — à condition d’être pratiquée avec rigueur, totalement individualisée sur la base d’un bilan biologique et holistique complet, et inscrite dans la durée.
Les perspectives ouvertes par la métabolomique, l’épigénétique nutritionnelle et la médecine de précision laissent entrevoir un futur proche où chaque profil de fatigue chronique pourra être adressé avec une précision moléculaire aujourd’hui encore inaccessible en routine. En attendant, les connaissances actuelles offrent déjà un cadre d’action solide, fondé sur les preuves, pour redonner à chaque patient les clés de son énergie.
Article du blog en lien avec la fatigue chronique :
- Alimentation anti-inflammatoire : lien
- La nutrition grande oubliée des médecins : lien
- Inflammation silencieuse : êtes-vous concerné ? : lien
Références scientifiques (sélection)
- Naviaux RK et al. — PNAS 2016 Article original sur PNAS : https://pubmed.ncbi.nlm.nih.gov/27573827/
- Giloteaux L et al. — Microbiome 2016 Article identifié sur PubMed : https://pubmed.ncbi.nlm.nih.gov/27338587/
- Sonnenburg JL et al. — Cell 2021 : https://pmc.ncbi.nlm.nih.gov/articles/PMC9020749/
- Fluge Ø & Mella O — BMC Neurology 2009 : https://pmc.ncbi.nlm.nih.gov/articles/PMC2711959/
- Shivappa N et al. — Public Health Nutrition 2014 : https://pubmed.ncbi.nlm.nih.gov/23941862/
- Tomas C et al. — PLOS ONE 2017 : https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0186802
- Guo C et al. — Cell Host & Microbe 2023 : https://pmc.ncbi.nlm.nih.gov/articles/PMC10183837/)


